بافر چیست و چگونه کار میکند؟
بافر یک محلول شیمیایی است که میتواند pH خود را در برابر افزودن اسید یا باز حفظ کند. این ویژگی بافر را برای کاربردهای متعددی در آزمایشگاه، صنعت، و پزشکی مفید میکند.
pH یک محلول
pH مقیاسی برای اندازهگیری اسیدیته یا قلیایی بودن یک محلول است. محلولهای اسیدی pH کمتر از 7 دارند، محلولهای قلیایی pH بیشتر از 7 دارند، و محلولهای خنثی pH 7 دارند.
تعادل اسید-باز
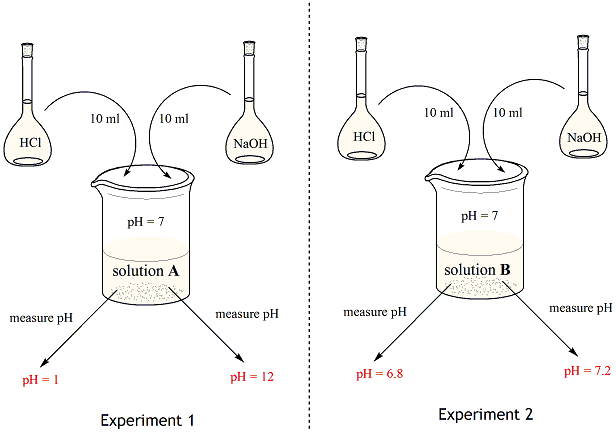
در یک محلول آبی، آب به صورت تعادلی بین یونهای H+ و OH- وجود دارد.
H2O <=> H+ + OH-
غلظت یونهای H+ و OH- در یک محلول آبی با هم برابر است و pH محلول را تعیین میکند.
نحوه کار بافر
بافر با استفاده از تعادل اسید-باز برای حفظ pH خود عمل میکند. بافر حاوی یک اسید ضعیف و نمک آن است.
هنگامی که اسید به یک محلول بافر اضافه میشود، اسید ضعیف با یونهای H+ اضافی واکنش میدهد و آنها را به شکل مولکولهای آب تبدیل میکند.
HA + H+ <=> H3O+
این واکنش باعث میشود که غلظت یونهای H+ در محلول کاهش یابد و pH محلول ثابت بماند.
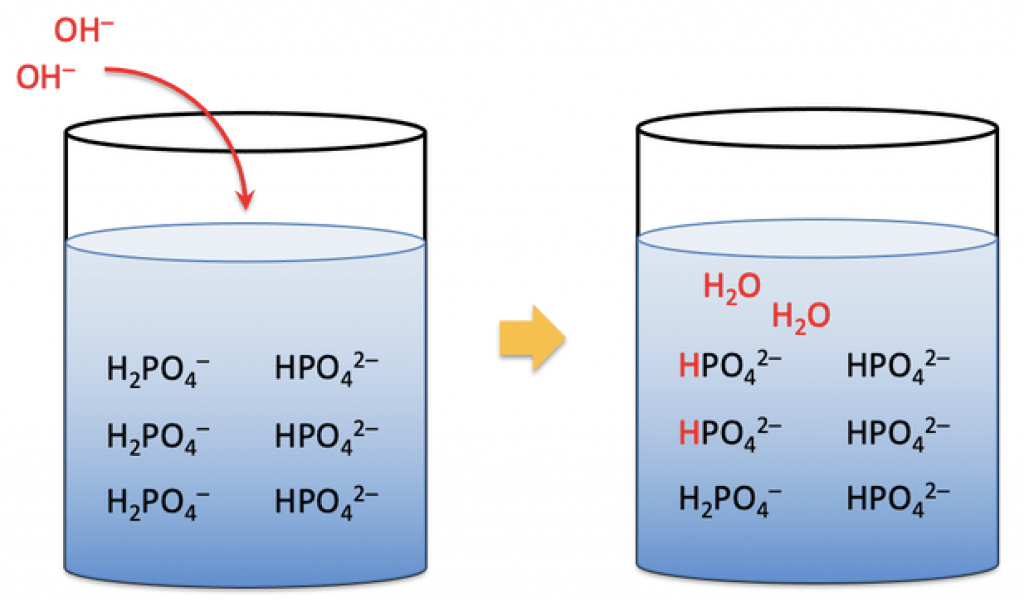
هنگامی که باز به یک محلول بافر اضافه میشود، یونهای OH- اضافی با اسید ضعیف واکنش میدهند و آن را به شکل نمک تبدیل میکنند.
HA + OH- <=> H2O + A-
این واکنش باعث میشود که غلظت یونهای OH- در محلول کاهش یابد و pH محلول ثابت بماند.
انواع بافر
بافرهای مختلفی وجود دارند که از نظر نوع اسید ضعیف و نمک آن با هم تفاوت دارند. برخی از انواع رایج بافر عبارتند از:
- بافر استیک اسید-استیک انیدرید: این بافر از اسید استیک و استیک انیدرید تشکیل شده است.
- بافر فسفات: این بافر از اسید فسفات و نمکهای آن تشکیل شده است.
- بافر سیترات: این بافر از اسید سیتریک و نمکهای آن تشکیل شده است.
کاربردهای بافر
بافر دارای کاربردهای فراوانی در آزمایشگاه، صنعت، و پزشکی است. برخی از کاربردهای رایج بافر عبارتند از:
- حفظ pH در آزمایشات: بافر برای حفظ pH در آزمایشات مختلف، مانند آزمایشهای بیوشیمیایی و زیستشناسی سلولی، استفاده میشود.
- کنترل pH در صنایع: بافر برای کنترل pH در صنایع مختلف، مانند صنایع غذایی، داروسازی، و شیمیایی، استفاده میشود.
- اصلاح pH بدن: بافر برای اصلاح pH بدن در شرایط پزشکی خاص، مانند اسیدوز و آلکالوز، استفاده میشود.
نتیجهگیری
بافر یک محلول شیمیایی با کاربردهای فراوان است. بافر با استفاده از تعادل اسید-باز برای حفظ pH خود عمل میکند. بافر دارای کاربردهای گستردهای در آزمایشگاه، صنعت، و پزشکی است.
میانبند
در متن بالا، بافر به عنوان یک محلول شیمیایی معرفی شد که میتواند pH خود را در برابر افزودن اسید یا باز حفظ کند. بافر با استفاده از تعادل اسید-باز برای حفظ pH خود عمل میکند.
در این میانبند، به بررسی دقیقتر نحوه کار بافر خواهیم پرداخت. همچنین، به برخی از کاربردهای مهم بافر نیز خواهیم پرداخت.
نحوه کار بافر
همانطور که در متن بالا ذکر شد، بافر حاوی یک اسید ضعیف و نمک آن است. اسید ضعیف میتواند به صورت یونهای H+ و A- وجود داشته باشد. نمک اسید ضعیف نیز میتواند به صورت یونهای A- و آنیونهای دیگر وجود داشته باشد.
هنگامی که اسید به یک محلول بافر اضافه میشود، اسید ضعیف با یونهای H+ اضافی واکنش میدهد و آنها را به شکل مولکولهای آب تبدیل میکند.
HA + H+ <=> H3O+
این واکنش باعث میشود که غلظت یونهای H+ در محلول کاهش یابد و pH محلول ثابت بماند.
هنگامی که باز به یک محلول بافر اضافه میشود، یونهای OH- اضافی با اسید ضعیف واکنش میدهند و آن را به شکل نمک تبدیل میکنند.
HA + OH- <=> H2O + A-
این واکنش باعث میشود که غلظت یونهای OH- در محلول کاهش یابد و pH محلول ثابت بماند.
کاربردهای مهم بافر
بافر دارای کاربردهای فراوانی در آزمایشگاه، صنعت، و پزشکی است. برخی از کاربردهای مهم بافر عبارتند از:
- حفظ pH در آزمایشات: بافر برای حفظ pH در آزمایشات مختلف، مانند آزمایشهای بیوشیمیایی و زیستشناسی سلولی، استفاده میشود.
pH یک عامل مهم در بسیاری از واکنشهای شیمیایی است. بافر میتواند pH را در یک محدوده خاص حفظ کند، که به واکنشها اجازه میدهد به طور صحیح انجام شوند.
- کنترل pH در صنایع: بافر برای کنترل pH در صنایع مختلف، مانند صنایع غذایی، داروسازی، و شیمیایی، استفاده میشود.
pH نقش مهمی در کیفیت محصولات غذایی و دارویی دارد. بافر میتواند pH را در یک محدوده مطلوب حفظ کند، که به بهبود کیفیت محصولات کمک میکند.
- اصلاح pH بدن: بافر برای اصلاح pH بدن در شرایط پزشکی خاص، مانند اسیدوز و آلکالوز، استفاده میشود.
pH بدن باید در یک محدوده خاص حفظ شود تا عملکرد صحیح بدن تضمین شود. بافر میتواند pH بدن را در شرایط پزشکی خاص اصلاح کند، که به بهبود سلامتی کمک میکند.
نتیجهگیری
بافر یک محلول شیمیایی با کاربردهای فراوان است. بافر با استفاده از تعادل اسید-باز برای حفظ pH خود عمل میکند. بافر دارای کاربردهای گستردهای در آزمایشگاه، صنعت، و پزشکی است.
افزودههای میانبند
در این میانبند، به برخی از نکات مهم زیر نیز پرداخته شد:
- انواع بافر: بافرهای مختلفی وجود دارند که از نظر نوع اسید ضعیف و نمک آن با هم تفاوت دارند.
- pH بافر: pH یک محلول بافر توسط غلظت اسید ضعیف و نمک آن تعیین میشود.
- قدرت بافر: قدرت بافر به میزان توانایی آن در حفظ pH در برابر افزودن اسید یا باز بستگی دارد.
امیدوارم این میانبند برای شما مفید باشد.
میانبند دوم
در میانبند اول، به بررسی نحوه کار بافر و برخی از کاربردهای مهم آن پرداختیم. در این میانبند، به بررسی عمیقتر برخی از کاربردهای بافر در آزمایشگاه، صنعت، و پزشکی خواهیم پرداخت.
کاربرد بافر در آزمایشگاه
بافر در آزمایشگاه برای حفظ pH در آزمایشات مختلف استفاده میشود. pH یک عامل مهم در بسیاری از واکنشهای شیمیایی است. بافر میتواند pH را در یک محدوده خاص حفظ کند، که به واکنشها اجازه میدهد به طور صحیح انجام شوند.
برخی از کاربردهای خاص بافر در آزمایشگاه عبارتند از:
- حفظ pH در واکنشهای بیوشیمیایی: بسیاری از واکنشهای بیوشیمیایی در یک pH خاص انجام میشوند. بافر میتواند pH را در این واکنشها ثابت نگه دارد، که به عملکرد صحیح آنها کمک میکند.
- کنترل pH در آزمایشهای بیولوژیکی: pH نقش مهمی در بسیاری از آزمایشهای بیولوژیکی دارد. بافر میتواند pH را در این آزمایشها ثابت نگه دارد، که به دقت نتایج کمک میکند.
- اندازهگیری pH: بافر میتواند برای اندازهگیری pH استفاده شود. با افزودن یک بافر به یک محلول، میتوان pH آن را با استفاده از یک pH متر اندازهگیری کرد.
کاربرد بافر در صنعت
بافر در صنعت برای کنترل pH در محصولات مختلف استفاده میشود. pH نقش مهمی در کیفیت محصولات غذایی و دارویی دارد. بافر میتواند pH را در یک محدوده مطلوب حفظ کند، که به بهبود کیفیت محصولات کمک میکند.
برخی از کاربردهای خاص بافر در صنعت عبارتند از:
- کنترل pH در صنایع غذایی: pH بر طعم، رنگ، و ماندگاری بسیاری از محصولات غذایی تأثیر میگذارد. بافر میتواند pH را در این محصولات ثابت نگه دارد، که به بهبود کیفیت آنها کمک میکند.
- کنترل pH در صنایع دارویی: pH بر پایداری و اثربخشی بسیاری از داروها تأثیر میگذارد. بافر میتواند pH را در این داروها ثابت نگه دارد، که به بهبود کیفیت آنها کمک میکند.
- کنترل pH در صنایع شیمیایی: pH بر واکنشهای شیمیایی مختلفی که در صنایع شیمیایی استفاده میشوند تأثیر میگذارد. بافر میتواند pH را در این واکنشها ثابت نگه دارد، که به بهبود عملکرد آنها کمک میکند.
کاربرد بافر در پزشکی
بافر در پزشکی برای اصلاح pH بدن در شرایط پزشکی خاص استفاده میشود. pH بدن باید در یک محدوده خاص حفظ شود تا عملکرد صحیح بدن تضمین شود. بافر میتواند pH بدن را در شرایط پزشکی خاص اصلاح کند، که به بهبود سلامتی کمک میکند.
برخی از کاربردهای خاص بافر در پزشکی عبارتند از:
- اصلاح اسیدوز و آلکالوز: اسیدوز و آلکالوز شرایطی هستند که در آن pH بدن از حد طبیعی خارج میشود. بافر میتواند pH بدن را در این شرایط اصلاح کند، که به بهبود سلامتی کمک میکند.
- حفظ pH خون: pH خون باید در یک محدوده خاص حفظ شود تا عملکرد صحیح اندامها و بافتها تضمین شود. بافر میتواند pH خون را در این محدوده حفظ کند، که به بهبود سلامتی کمک میکند.
نتیجهگیری
بافر یک محلول شیمیایی با کاربردهای فراوان است. بافر دارای کاربردهای گستردهای در آزمایشگاه، صنعت، و پزشکی است.
افزودههای میانبند دوم
در این میانبند، به برخی از نکات مهم زیر نیز پرداخته شد:
- انواع بافر برای کاربردهای مختلف: بافرهای مختلفی وجود دارند که برای کاربردهای مختلف مناسب هستند.
- نحوه انتخاب بافر مناسب: برای انتخاب بافر مناسب، باید به عوامل مختلفی، مانند pH مورد نظر، قدرت بافر، و هزینه، توجه کرد.
امیدوارم این میانبند برای شما مفید باشد.
میانبند سوم
در میانبند اول و دوم، به بررسی کلی بافر و کاربردهای آن پرداختیم. در این میانبند، به بررسی برخی از کاربردهای پیشرفته بافر خواهیم پرداخت.
کاربردهای پیشرفته بافر
بافر دارای کاربردهای پیشرفتهای نیز هست که در اینجا به برخی از آنها اشاره میشود:
- کنترل pH در سلولهای زنده: بافر نقش مهمی در حفظ pH سلولهای زنده ایفا میکند. pH سلولهای زنده باید در یک محدوده خاص حفظ شود تا عملکرد صحیح آنها تضمین شود. بافر میتواند pH سلولهای زنده را در این محدوده حفظ کند، که به بهبود سلامت سلولها کمک میکند.
- اصلاح pH در محیط زیست: بافر میتواند برای اصلاح pH در محیط زیست استفاده شود. pH محیط زیست میتواند تحت تأثیر عوامل مختلفی، مانند فعالیتهای انسانی، تغییر کند. بافر میتواند pH محیط زیست را در یک محدوده مطلوب حفظ کند، که به حفظ اکوسیستمها کمک میکند.
- ساخت مواد جدید: بافر میتواند برای ساخت مواد جدید استفاده شود. مواد جدیدی که با استفاده از بافر ساخته میشوند، دارای خواص مختلفی هستند که میتوانند در کاربردهای مختلف استفاده شوند.
نتیجهگیری
بافر یک محلول شیمیایی با کاربردهای فراوان است. بافر دارای کاربردهای گستردهای در آزمایشگاه، صنعت، و پزشکی است. همچنین، بافر دارای کاربردهای پیشرفتهای نیز هست که در آینده میتواند کاربردهای بیشتری پیدا کند.
افزودههای میانبند سوم
در این میانبند، به برخی از نکات مهم زیر نیز پرداخته شد:
- کاربردهای بافر در زیستشناسی: بافر نقش مهمی در زیستشناسی ایفا میکند. بافر به حفظ pH سلولهای زنده، تنظیم pH خون، و سایر فرآیندهای زیستی کمک میکند.
- کاربردهای بافر در محیط زیست: بافر میتواند برای حفظ pH آبهای زیرزمینی، دریاها، و سایر منابع آبی استفاده شود.
- کاربردهای بافر در ساخت مواد جدید: بافر میتواند برای ساخت مواد جدیدی با خواص مختلفی، مانند مواد زیستفعال، مواد هوشمند، و مواد کامپوزیتی، استفاده شود.
امیدوارم این میانبند برای شما مفید باشد.
میانبند چهارم
در میانبند اول تا سوم، به بررسی کلی بافر و کاربردهای آن پرداختیم. در این میانبند، به بررسی برخی از چالشهای مرتبط با بافر خواهیم پرداخت.
چالشهای مرتبط با بافر
بافر یک محلول شیمیایی نسبتاً ساده است، اما با این حال، برخی از چالشهای مرتبط با آن وجود دارد. برخی از این چالشها عبارتند از:
- انتخاب بافر مناسب: انتخاب بافر مناسب برای یک کاربرد خاص میتواند چالشبرانگیز باشد. عوامل مختلفی، مانند pH مورد نظر، قدرت بافر، و هزینه، باید در نظر گرفته شوند.
- پایداری بافر: برخی از بافرها پایدارتر از بافرهای دیگر هستند. پایداری بافر به عوامل مختلفی، مانند دما، pH، و وجود سایر مواد شیمیایی، بستگی دارد.
- ایمنی بافر: برخی از بافرها میتوانند برای سلامتی مضر باشند. هنگام استفاده از بافر باید اقدامات احتیاطی لازم انجام شود.
چالشهای انتخاب بافر مناسب
انتخاب بافر مناسب برای یک کاربرد خاص میتواند چالشبرانگیز باشد. عوامل مختلفی، مانند pH مورد نظر، قدرت بافر، و هزینه، باید در نظر گرفته شوند.
- pH مورد نظر: pH بافر باید با pH مورد نظر برای کاربرد خاص مطابقت داشته باشد.
- قدرت بافر: قدرت بافر به میزان توانایی آن در حفظ pH در برابر افزودن اسید یا باز بستگی دارد. قدرت بافر باید با نیازهای کاربرد خاص مطابقت داشته باشد.
- هزینه: هزینه بافر میتواند یک عامل مهم باشد.
چالشهای پایداری بافر
برخی از بافرها پایدارتر از بافرهای دیگر هستند. پایداری بافر به عوامل مختلفی، مانند دما، pH، و وجود سایر مواد شیمیایی، بستگی دارد.
- دمای بالا: دمای بالا میتواند پایداری برخی از بافرها را کاهش دهد.
- pH پایین: pH پایین میتواند پایداری برخی از بافرها را کاهش دهد.
- حضور سایر مواد شیمیایی: برخی از مواد شیمیایی میتوانند با بافرها واکنش دهند و پایداری آنها را کاهش دهند.
چالشهای ایمنی بافر
برخی از بافرها میتوانند برای سلامتی مضر باشند. هنگام استفاده از بافر باید اقدامات احتیاطی لازم انجام شود.
- سمیت: برخی از بافرها میتوانند سمی باشند.
- حساسیت پوستی: برخی از بافرها میتوانند باعث حساسیت پوستی شوند.
- حساسیت تنفسی: برخی از بافرها میتوانند باعث حساسیت تنفسی شوند.
نتیجهگیری
بافر یک محلول شیمیایی با کاربردهای فراوان است. با این حال، برخی از چالشهای مرتبط با آن وجود دارد. آگاهی از این چالشها میتواند به انتخاب و استفاده ایمن از بافر کمک کند.
افزودههای میانبند چهارم
در این میانبند، به برخی از نکات مهم زیر نیز پرداخته شد:
- راههای کاهش چالشهای مرتبط با بافر: برخی از راههای کاهش چالشهای مرتبط با بافر عبارتند از:
- استفاده از بافر مناسب برای کاربرد خاص
- ذخیره بافر در شرایط مناسب
- استفاده از تجهیزات ایمنی هنگام کار با بافر
امیدوارم این میانبند برای شما مفید باشد.
نتیجهگیری
بافر یک محلول شیمیایی با کاربردهای فراوان است. بافر با استفاده از تعادل اسید-باز برای حفظ pH خود عمل میکند. بافر دارای کاربردهای گستردهای در آزمایشگاه، صنعت، و پزشکی است. همچنین، بافر دارای کاربردهای پیشرفتهای نیز هست که در آینده میتواند کاربردهای بیشتری پیدا کند.
اهمیت بافر
بافر یک ابزار مهم در بسیاری از زمینهها است. بافر میتواند به حفظ pH در یک محدوده خاص کمک کند، که میتواند برای عملکرد صحیح بسیاری از فرآیندهای شیمیایی، بیولوژیکی، و پزشکی ضروری باشد.
چالشهای مرتبط با بافر
با وجود کاربردهای فراوان، بافر برخی از چالشهای مرتبط با خود را نیز دارد. برخی از این چالشها عبارتند از:
- انتخاب بافر مناسب: انتخاب بافر مناسب برای یک کاربرد خاص میتواند چالشبرانگیز باشد.
- پایداری بافر: برخی از بافرها پایدارتر از بافرهای دیگر هستند.
- ایمنی بافر: برخی از بافرها میتوانند برای سلامتی مضر باشند.
راههای کاهش چالشهای مرتبط با بافر
آگاهی از چالشهای مرتبط با بافر میتواند به انتخاب و استفاده ایمن از بافر کمک کند. برخی از راههای کاهش چالشهای مرتبط با بافر عبارتند از:
- استفاده از بافر مناسب برای کاربرد خاص
- ذخیره بافر در شرایط مناسب
- استفاده از تجهیزات ایمنی هنگام کار با بافر
آینده بافر
بافر یک فناوری با پتانسیل رشد است. بافر میتواند در کاربردهای جدیدی استفاده شود و کاربردهای موجود آن نیز میتواند گسترش یابد.
بافر یک ابزار قدرتمند است که میتواند برای بهبود کیفیت زندگی انسانها استفاده شود. بافر میتواند برای حفظ pH در غذاها و داروها استفاده شود، که میتواند به بهبود طعم، ماندگاری، و ایمنی آنها کمک کند. بافر همچنین میتواند برای کنترل pH در محیط زیست استفاده شود، که میتواند به حفظ اکوسیستمها کمک کند.
در آینده، بافر میتواند در کاربردهای جدیدی استفاده شود. به عنوان مثال، بافر میتواند برای ساخت مواد جدید با خواص بهبود یافته استفاده شود. بافر همچنین میتواند برای توسعه روشهای درمانی جدید برای بیماریها استفاده شود.
با توجه به کاربردهای فراوان و پتانسیل رشد بافر، این فناوری میتواند نقش مهمی در بهبود کیفیت زندگی انسانها در آینده ایفا کند.
در اینجا به برخی از کاربردهای جدید احتمالی بافر اشاره میشود:
- ساخت مواد زیستفعال: بافر میتواند برای ساخت مواد زیستفعال استفاده شود که میتوانند با بدن انسان تعامل داشته باشند. این مواد میتوانند برای اهداف مختلفی، مانند درمان بیماریها، بهبود عملکرد اندامها، و افزایش طول عمر، استفاده شوند.
- توسعه روشهای درمانی جدید: بافر میتواند برای توسعه روشهای درمانی جدید برای بیماریها استفاده شود. به عنوان مثال، بافر میتواند برای اصلاح pH در بافتهای آسیبدیده استفاده شود، که میتواند به بهبود روند بهبود کمک کند.
- کنترل آلودگی محیط زیست: بافر میتواند برای کنترل آلودگی محیط زیست استفاده شود. به عنوان مثال، بافر میتواند برای جذب آلایندهها از آب و هوا استفاده شود.
با پیشرفت تحقیقات در مورد بافر، کاربردهای جدید و نوآورانهای برای این فناوری کشف خواهد شد.
برای خواندن درباره “هیدروفلوئوریک اسید: یک ماده شیمیایی خطرناک و مفید” روی لینک کلیک کنید

